宫颈冷刀锥切术
宫颈冷刀锥切术(cold knife conization,CKC)就是将宫颈阴道部及部分宫颈管做圆锥形切除,是一种古老的妇科手术,已有近一百八十年的历史。随着宫颈上皮内瘤变(cervical intraepithelial neoplasia,CIN)发生率的升高和宫颈癌患者的年轻化,宫颈锥切术越来越显示出其特有的临床应用价值。根据手术的目的不同,宫颈锥切术可分为两种:诊断性宫颈锥切术和治疗性宫颈锥切术。
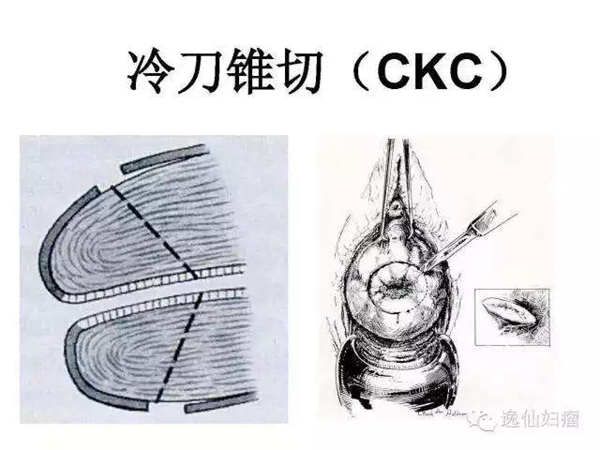
在阴道镜应用前,绝大多数宫颈细胞学异常者要施行诊断性宫颈锥切术以明确诊断。由于阴道镜检查及镜下多点活检具有手术时间短、出血少、患者痛苦少和术后并发症少等优点,因此,阴道镜技术在诊断宫颈病变中得以大力推广,致使诊断性宫颈锥切术的临床应用曾一度大为减少,大有被阴道镜检查及镜下多点活检取代之势。近年发现阴道镜检查及镜下宫颈多点活检不能完全代替诊断性宫颈锥切,其原因为:
①阴道镜检查不能发现宫颈管内的病变;
②CIN常常是多灶性的,阴道镜下宫颈活检的组织有限,容易造成漏诊;
③阴道镜下多点活检诊断宫颈病变(≥CINⅡ)的敏感性和特异性偏低,分别为81.0%和77.0%,可致CIN诊断过高或过低;
④阴道镜检查难以鉴别宫颈原位癌和微小浸润癌。文献报告16.7%~22.2%的患者阴道镜下活检病理诊断的结果较宫颈锥切的诊断结果轻(沈铿等,2001;郎景和等,2001;张洵等,2003)。
诊断性宫颈冷刀锥切术的指征
近年,越来越多的临床医师喜欢用高频电刀(LEEP)或普通电刀行宫颈锥切术,但在以下情况应行冷刀锥切,而不宜行LEEP锥切术:
①宫颈细胞学检查为HSIL,阴道镜检查阴性或不满意;
②阴道镜检未看到病变的边界或未见鳞柱交界上界;
③主要病灶位于宫颈管内或高度宫颈病变延伸入颈管内,超出阴道镜检查的范围;
④宫颈细胞学诊断较阴道镜下宫颈活检的病理结果重(相差2级);
⑤宫颈管刮术(ECC)的病理结果为异常或不能确定;
⑥宫颈细胞学提示腺上皮异常或可疑宫颈腺癌或宫颈原位腺癌;
⑦宫颈活检病理提示可疑微小浸润癌者;
⑧细胞学、阴道镜怀疑宫颈浸润癌,但活检病理未能证实者;
⑨外宫颈病变范围广,累及宫颈四象限,甚至延伸至阴道穹隆者。而妊娠期内的宫颈HSIL(≥CINⅡ)患者是冷刀锥切的相对禁忌证(章文华,2011)。
冷刀锥切术的优缺点
目前常用的诊断性锥切术式包括:冷刀锥切术(CKC)、LEEP锥切术和普通电刀锥切术等。而冷刀锥切术是一种传统、经典的宫颈锥切术,常作为评价其他锥切手术的标准。
冷刀锥切具有下列优势:
①可一次性切除足够大的、完整的宫颈标本用于组织病理学诊断,且锥切标本边缘病变的切净率较高。有一组报告CKC宫颈标本的平均锥高(18.9mm)和标本边缘的切净率(100%),明显高于LEEP锥切标本(12.8mm和80%),且对于病变范围大的患者常需多次电圈切除,可能影响组织病理学诊断的准确性。
②CKC不影响切除标本边缘组织的病理诊断,而LEEP锥切术后标本的切缘组织受电热反应的破坏,影响病理诊断。文献报道LEEP锥切标本切缘的热损伤率可达50%以上,平均热损伤的深度:宫颈外切缘为0.98mm,内切缘为0.95mm;LEEP锥切术后约有7%~8.3%的标本切缘组织的病理诊断不能确定(Giacalone PL等,1999;樊庆泊等,2001)。
③CKC可用于腺上皮异常患者的诊断。
冷刀锥切有以下缺点:
①需住院手术,平均住院时间6~8天,明显长于激光锥切术的手术时间(平均0.6天)(Moriyama M等,1991);
②手术费时,平均手术时间(28.1分钟),长于激光锥切手术(15分钟)和LEEP术(5.4分钟)(Moriyama M等,1991;Duggan BD等,1999);
③一般需在全麻或局部麻醉下手术;
④并发症较多。因此,诊断性冷刀锥切的适应证应严格掌握。
诊断性冷刀锥切的临床意义
(1)明确宫颈病变的严重程度,确定或排除宫颈的镜下浸润癌或浸润癌。
(2)明确宫颈病变是否为原位腺癌。
(3)明确病变累及宫颈管的深度或颈管病变的深度。
(4)指导术后进一步治疗或追踪。
Kliemann LK等(2012)报道阴道镜检查不满意的CIN2/3患者,通过诊断性锥切可以发现7%的隐匿性宫颈浸润癌。






 2022
2022